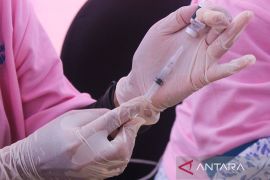
Keamanan vaksin AWcorna secara umum dapat ditoleransi dengan baik
Jakarta (ANTARA) - Kepala Badan Pengawas Obat dan Makanan (BPOM) RI Penny K Lukito mengatakan AWcorna menjadi merek dagang pertama vaksin COVID-19 berplatform mRNA yang dikembangkan dan diproduksi di Indonesia.
"Dengan disetujuinya Izin Penggunaan Darurat (EUA) terhadap vaksin ini, semakin menambah alternatif vaksin yang dapat digunakan dalam program Vaksinasi COVID-19 untuk dewasa usia 18 tahun ke atas," kata Penny K Lukito dalam konferensi pers pemberian EUA vaksin produksi dalam negeri di Gedung BPOM RI, Jakarta, Jumat.
AWcorna didaftarkan oleh perusahaan farmasi swasta PT Etana Biotechnologies Indonesia (PT Etana) dan dikembangkan melalui transfer teknologi dan penelitian bersama Abogen-Yuxi Walvax, China.
Pengembangan platform mRNA itu dilakukan di fasilitas produksi PT Etana yang berdomisili di kawasan Pulogadung, Jakarta Timur.
Baca juga: BPOM pastikan seluruh vaksin COVID-19 produksi dalam negeri halal
Baca juga: BPOM setujui tiga vaksin COVID-19 untuk anak di Indonesia
Vaksin mRNA (messenger RNA) merupakan vaksin jenis terbaru yang kandungannya berbeda dengan jenis vaksin lainnya. Jika vaksin konvensional mengandung virus atau kuman penyebab penyakit yang telah dilemahkan atau dimatikan, tapi vaksin mRNA merupakan vaksin dengan teknologi terbaru hasil pengembangan bio teknologi.
Jumlah produsen vaksin berplatform berbasis komputerisasi itu juga masih terbatas di dunia, di antaranya Vaksin Pfizer dan Moderna asal Amerika Serikat.
"Hal penting yang perlu menjadi perhatian, terutama oleh pihak sarana distribusi dan fasilitas pelayanan kesehatan adalah proses penyimpanan Vaksin AWcorna. Walaupun termasuk vaksin platform mRNA, vaksin ini dapat disimpan pada suhu 2 hingga 8 derajat Celcius," katanya
AWcorna memiliki kelebihan dari vaksin berplatform serupa karena standar suhu penyimpanan telah tersedia hampir di seluruh daerah.
Sementara vaksin lainnya membutuhkan fasilitas penyimpanan rantai dingin pada suhu yang sangat rendah, yaitu minus 70 derajat Celsius atau lebih rendah yang masih terbatas jumlahnya di Indonesia.
Penny mengatakan AWcorna telah memenuhi aspek keamanan, efikasi/imunogenisitas, mutu, dan pemenuhan prinsip Cara Pembuatan Obat yang Baik (CPOB).
Vaksin AWcorna disetujui mendapatkan EUA untuk indikasi pencegahan infeksi virus SARS CoV-2 pada individu usia 18 tahun ke atas.
Dosis sebagai vaksinasi primer adalah 15 μg/dosis yang diberikan dalam 2 dosis suntikan dengan interval 28 hari.
Sebagai vaksin booster heterolog, diberikan dalam satu dosis sebanyak 15 μg/dosis setelah 6 bulan dosis kedua vaksinasi primer dengan menggunakan vaksin inaktivasi (Sinovac atau Sinopharm).
Dari hasil uji klinik, kata Penny, efikasi Vaksin AWcorna terhadap wild type (virus COVID-19 yang belum bermutasi) sebesar 83,58 persen, sementara efikasi Vaksin AWcorna terhadap varian Omicron sebesar 71,17 persen dalam mencegah kasus COVID-19 sedang (moderate).
"Keamanan vaksin AWcorna secara umum dapat ditoleransi dengan baik dan efek samping yang dilaporkan berisifat ringan," katanya.
Baca juga: BPOM: Swasta rintis produksi vaksin lokal mRNA via transfer teknologi
Baca juga: Bio Farma targetkan vaksin COVID-19 Indovac dapat izin BPOM September
Pewarta: Andi Firdaus
Editor: Zita Meirina
Copyright © ANTARA 2022