Obat diberikan dua kali sehari sebanyak empat kapsul masing-masing 200 mg selama lima hariJakarta (ANTARA) - Badan Pengawas Obat dan Makanan (BPOM) RI menerbitkan Izin Penggunaan Darurat (Emergency Use Authorization/EUA) untuk obat antivirus COVID-19 Molnupiravir.
"Setelah melalui evaluasi terhadap data hasil uji klinik bersama dengan Tim Ahli Komite Nasional Penilai Obat serta asosiasi klinisi untuk persetujuan EUA ini, BPOM bersama Kementerian Kesehatan terus memantau keamanan penggunaan Molnupiravir di Indonesia,” ujar Kepala BPOM RI Penny K Lukito melalui siaran pers yang diterima di Jakarta, Jumat.
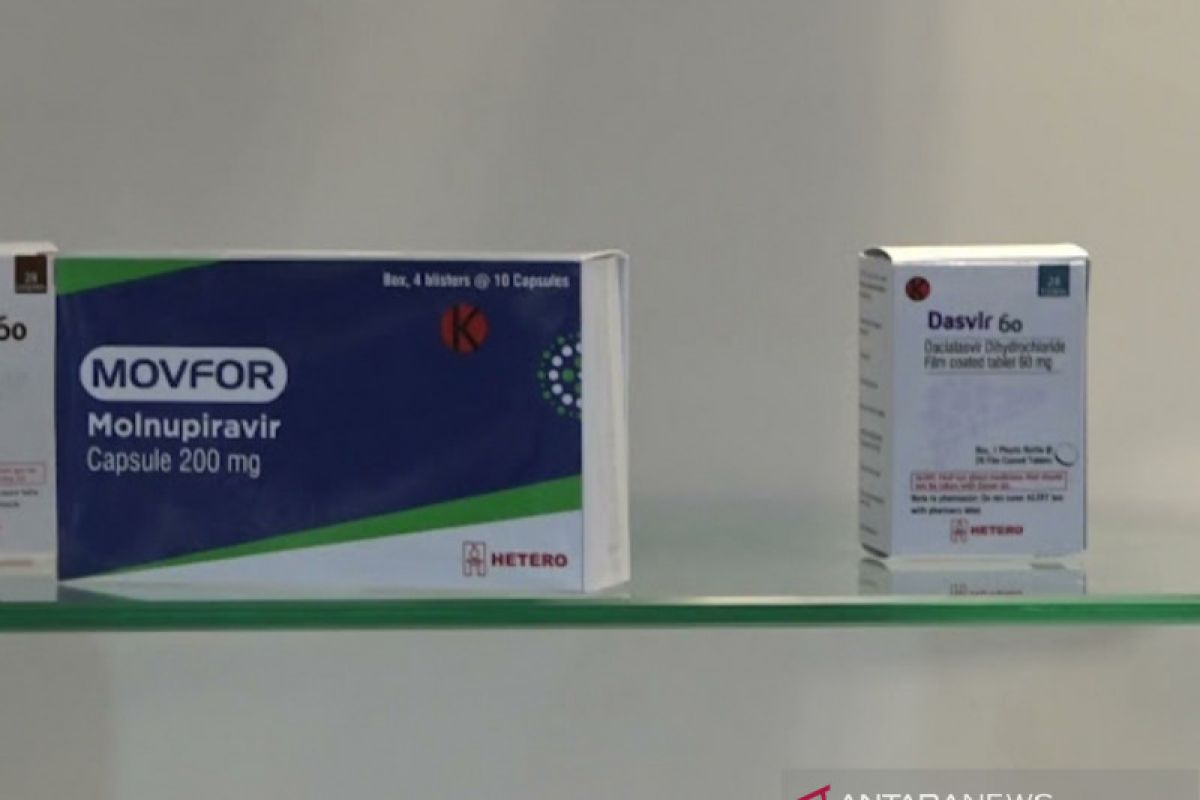
Penny mengatakan Molnupiravir yang disetujui berupa kapsul 200 mg yang didaftarkan oleh PT Amarox Pharma Global dan diproduksi Hetero Labs Ltd, India.
Baca juga: Obat antivirus Molnupiravir diproduksi di Indonesia April 2022
Obat itu diindikasikan untuk pengobatan infeksi COVID-19 ringan sampai sedang pada pasien usia 18 tahun ke atas yang tidak memerlukan pemberian oksigen dan memiliki peningkatan risiko menjadi infeksi COVID-19 berat.
"Obat diberikan dua kali sehari sebanyak empat kapsul masing-masing 200 mg selama lima hari," katanya.
Sebelumnya, BPOM telah menerbitkan EUA untuk beberapa obat COVID-19 di antaranya antivirus Favipiravir, antivirus Remdesivir, antibodi monoklonal Regdanvimab dan kini Molnupiravir.
Baca juga: Tiga perusahaan farmasi Indonesia bersiap impor obat Molnupiravir
Molnupiravir dikembangkan oleh Merck Sharp & Dohme (MSD). Selanjutnya MSD telah memberikan voluntary licensing (VL) kepada beberapa produsen di India, salah satunya Hetero Labs Ltd, India untuk memenuhi akses kebutuhan suplai global dengan cepat dan tetap memperhatikan mutu serta memberikan pilihan terhadap harga yang kompetitif.
Penny mengatakan hasil evaluasi dari aspek keamanan, pemberian Molnupiravir relatif aman dan memberikan efek samping yang dapat ditoleransi. Efek samping yang paling sering dilaporkan adalah mual, sakit kepala, mengantuk, nyeri abdomen dan nyeri orofaring.
Baca juga: BPOM targetkan EUA Vaksin Merah Putih Unair terbit Juni 2022
Selain itu, Hasil uji non-klinik dan uji klinik, molnupiravir tidak menyebabkan gangguan fungsi hati. Molnupiravir tidak boleh digunakan pada wanita hamil dan untuk wanita usia subur yang tidak hamil harus menggunakan kontrasepsi selama pemberian Molnupiravir.
Terkait aspek efikasi, kata Penny, hasil uji klinik fase tiga menunjukkan Molnupiravir dapat menurunkan risiko hospitalisasi atau risiko dirawat di rumah sakit bahkan kematian sebesar 30 persen pada pasien COVID-19 derajat ringan hingga sedang dan 24,9 persen pada pasien COVID-19 ringan.
Baca juga: BPOM: Daya tahan vaksin penguat diketahui usai 28 hari penyuntikan
Dalam mendukung ketersediaan obat COVID-19 di Indonesia, PT Amarox Pharma Global sedang melakukan persiapan produksi lokal Molnupiravir kapsul melalui teknologi transfer di fasilitas produksi Amarox Cikarang, Kabupaten Bekasi, Jawa Barat.
“Surat persetujuan penggunaan fasilitas produksi kapsul nonbetalaktam telah diterbitkan pada 3 Januari 2022, dan setelah persyaratan Cara Pembuatan Obat yang Baik (CPOB) dapat dipenuhi oleh industri maka produksi lokal direncanakan siap diproduksi pada awal Maret 2022. Hal ini semakin meningkatkan upaya kita bersama dalam mendukung kemandirian industri obat dalam negeri,” katanya.
Selain itu, BPOM juga melakukan pengawasan pada rantai produksi dan distribusi obat agar keamanan, khasiat, dan mutu obat yang beredar dapat dipertahankan serta dapat mencegah penggunaan obat ilegal.
Baca juga: BPOM terbitkan izin penggunaan darurat lima produk vaksin penguat
Baca juga: BPOM sebut vaksin Merah Putih diproduksi pada pertengahan 2022
Pewarta: Andi Firdaus
Editor: Agus Salim
Copyright © ANTARA 2022