Pengajuan Moderna kepada EU itu dilakukan beberapa minggu setelah menunda pengajuan serupa dengan regulator AS.
Uni Eropa pada Juli mengizinkan vaksin COVID buatan Moderna untuk digunakan pada remaja berusia 12 hingga 17 tahun.
Namun, beberapa negara termasuk Swedia menghentikan penggunaannya untuk orang berusia 30 tahun atau lebih muda karena efek samping terkait jantung yang jarang terjadi.
Baca juga: Moderna: FDA butuh waktu lebih lama meninjau vaksin COVID remaja
Pada akhir Oktober, Moderna mengatakan bahwa regulator obat Amerika Serikat membutuhkan lebih banyak waktu untuk menyelesaikan tinjauan tentang penggunaan vaksin Moderna pada kelompok usia 12-17 tahun.
Hal itu karena pihak regulator AS perlu mempelajari risiko jenis peradangan jantung yang disebut miokarditis setelah penggunaan vaksin.
Moderna menunda pengajuan izin penggunaan vaksin di AS untuk anak-anak berusia 6 hingga 11 tahun, sementara badan pengawas obat dan makanan AS (FDA) masih menyelesaikan tinjauannya untuk penggunaan vaksin pada kelompok usia 12 hingga 17 tahun.
Sebelumnya pada Oktober, Moderna mengatakan vaksinnya menghasilkan respons kekebalan yang kuat pada anak-anak berusia 6 hingga 11 tahun dan berencana untuk segera mengirimkan datanya ke para regulator global.
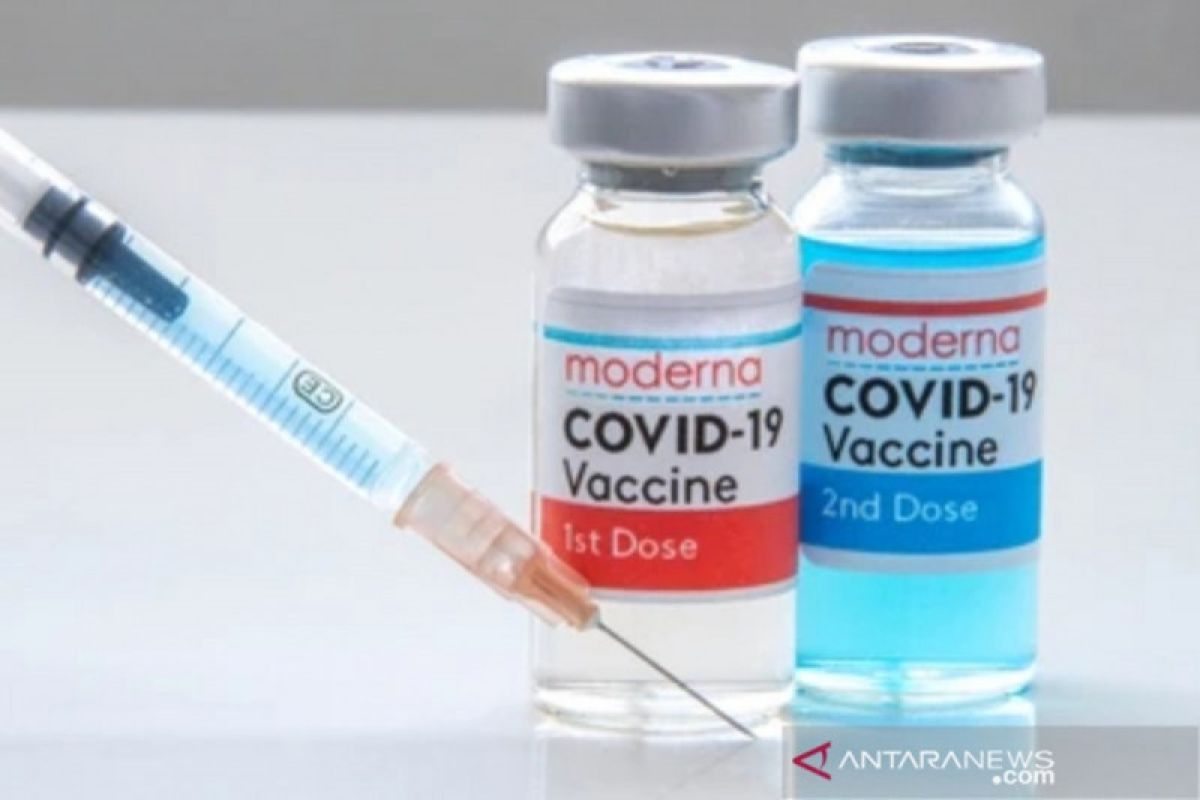
Moderna pada Selasa mengatakan bahwa pihaknya telah mengajukan permohonan kepada European Medicines Agency untuk penggunaan dosis vaksin 50 mikrogram pada anak-anak, yakni setengah dari dosis vaksin yang digunakan pada orang dewasa.
Sumber: Reuters
Baca juga: Prancis sarankan vaksin Moderna tidak untuk orang di bawah 30 tahun
Baca juga: Moderna pangkas prakiraan penjualan vaksin COVID-19 sepanjang 2021
Penerjemah: Yuni Arisandy Sinaga
Editor: Mulyo Sunyoto
Copyright © ANTARA 2021