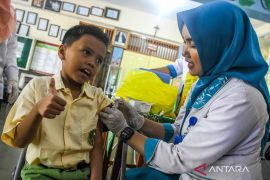
BPOM membuka peluang memakai data hasil uji klinis sejumlah vaksin COVID-19 dari negara lain guna mempercepat program vaksinasi di Indonesia.
Jakarta (ANTARA) - Badan Pengawas Obat dan Makanan (BPOM) sudah melakukan uji klinis terhadap vaksin Sinovac dan sudah memperoleh dua data setelah 2 bulan penyuntikan vaksin, yakni data immunogenitas dan efikasi yang menyatakan bahwa vaksin cukup aman.
"Dari data keamanan, vaksin ini sudah cukup aman. Tidak ada kejadian efek samping serius yang dilaporkan berkaitan dengan penggunaan vaksin ini," kata Juru Bicara Vaksinasi COVID-19 dari BPOM Lucia Rizka Andalusia, dalam keterangan tertulis, di Jakarta, Selasa.
Ia menjelaskan bahwa immunogenitas-nya juga sudah menunjukkan tingkat pembentukan antibodi yang bagus responsnya dalam tubuh
Hal tersebut disampaikannya dalam Alinea Forum bertajuk Kehalalan & Keamanan Vaksin COVID-19, Selasa. Dengan data itu bisa menepis keraguan masyarakat dalam menerima vaksin.
Saat ini, kata dia, BPOM masih menunggu sejumlah data uji klinis lainnya.
Baca juga: Presiden Jokowi dijadwalkan jalani vaksinasi COVID-19 pada 13 Januari
Lucia menyebutkan ada beberapa keuntungan yang diperoleh Indonesia dengan melakukan uji klinis, yakni mempunyai data uji klinis dan data pengalaman penggunaan di Indonesia.
Kendati demikian, BPOM membuka peluang memakai data hasil uji klinis sejumlah vaksin COVID-19 dari negara lain guna mempercepat program vaksinasi di Indonesia, asalkan syaratnya memiliki protokol uji klinis yang sama dengan Indonesia.
Menurut dia, sebenarnya tidak ada kewajiban melakukan uji klinis di dalam negeri sebelum menggunakan vaksin, apalagi bila ada negara tetangga yang sudah melakukan uji klinis sebelumnya.
Bahkan, kata dia, ada beberapa jenis vaksin yang telah digunakan di Indonesia, tanpa melalui uji klinis di Indonesia.
"Ingat, sudah banyak vaksin sebelum pandemi COVID-19, dan hanya sedikit yang melakukan uji klinis di Indonesia," katanya.
Ia mengatakan bahwa vaksin influenza dan vaksin polio uji klinisnya tidak di Indonesia. Meski diproduksi di Bio Farma, uji klinisnya tidak dilakukan di Indonesia dan secara regulasi memungkinkan.
Baca juga: BPOM pastikan bahan vaksin COVID-19 aman
Direktur Eksekutif Lembaga Pengkajian Pangan, Obat-obatan, dan Kosmetika Majelis Ulama Indonesia (LPPOM MUI) Muti Arintawati mengaku belum bisa menegaskan kehalalan vaksin Sinovac untuk menangkal COVID-19 karena masih ada informasi yang perlu dilengkapi.
Muti tidak membeberkan secara detail informasi yang dimaksud. Hanya kuantitasnya terbilang sedikit karena proses audit sudah rampung.
"Masih ada sedikit informasi yang harus dilengkapi sehingga tentunya kami tidak bisa kemudian memberikan kesimpulan. Kesimpulan halal tidaknya juga tidak ada di LPPOM, tetapi di Komisi Fatwa (MUI)," ujarnya.
LPPOM MUI memastikan tidak pasif dalam menerima informasi vaksin, tetapi secara intensif melakukan kajian yang dikerjakan auditor LPPOM MUI, seperti literatur, jurnal, dan keterangan pakar mengenai bahan baku vaksin juga digali.
"Kalau semua informasi sudah lengkap, MUI tetap menunggu keputusan dari BPOM tentang safety, tentang thoyyib tadi untuk memutuskan, kemudian apakah bisa dikeluarkan sertifikat halal atau tidak," katanya.
Baca juga: RS di AS diancam sanksi kalau lambat memvaksinasi pasien COVID-19
Sementara itu, Lembaga Bahtsul Masail Pengurus Besar Nahdlatul Ulama (LBM PBNU) memutuskan membolehkan penggunaan vaksin COVID-19 buatan Sinovac meskipun belum mengetahui kandungan zat pada bahan pokok pembuatan vaksin tersebut.
"Statemen Kiai Wapres (Wakil Presiden RI Ma'ruf Amin) menjadi pertimbangan kami untuk tidak melanjutkan pembahasan halal dan haramnya," kata Sekretaris LBM PBNU Sarmidi Husna.
Sarmidi berpandangan bahwa pernyataan Ma'ruf berlandaskan atas kegentingan situasi kehidupan akibat dampak COVID-19 sehingga penggunaan vaksin tidak berlabel halal dapat digunakan oleh umat Islam.
Pewarta: Zuhdiar Laeis
Editor: D.Dj. Kliwantoro
Copyright © ANTARA 2021