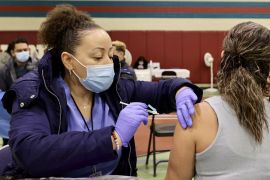
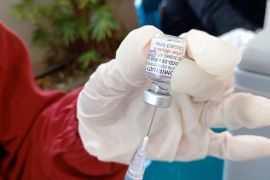
telah melalui serangkaian tahap preklinik dan uji klinik fase I dan II di Tiongkok
Jakarta (ANTARA) - Kepala Badan Pengawas Obat dan Makanan Penny K Lukito mengatakan bakal vaksin COVID-19 yang datang dari China masuk dengan mekanisme persetujuan pemasukan obat jalur khusus.
"Vaksin COVID-19 produksi Sinovac China yang diimpor ke Indonesia melalui mekanisme persetujuan pemasukan obat jalur khusus (special access scheme)," kata Penny kepada wartawan di Jakarta, Selasa.
BPOM, kata dia, juga akan memberikan pendampingan proses registrasi vaksin melalui mekanisme Emergency Use Authorization/EUA (Otorisasi Penggunaan Darurat) dengan persetujuan bersyarat untuk mempercepat akses vaksin COVID-19 sampai ke masyarakat.
Baca juga: Erick Thohir: Vaksin COVID-19 akan didaftarkan ke BPOM usai uji klinis
Baca juga: BPOM: Uji klinik kandidat vaksin COVID-19 ukur keamanan
Dia mengatakan vaksin COVID-19 Sinovac itu sedang dalam proses uji klinik fase III. Penelitian dan pengembangan vaksin itu melibatkan Biofarma dari Indonesia dan Sinovac (China).
Dalam kemitraan itu, dia mengatakan terjadi transfer teknologi untuk pengembangan produksi vaksin secara lokal dalam rangka memenuhi kebutuhan akses dan ketersediaan vaksin COVID-19 untuk masyarakat Indonesia.
"Vaksin COVID-19 Sinovac ini telah melalui serangkaian tahap preklinik dan uji klinik fase I dan II di Tiongkok. Berdasarkan hasil yang diperoleh dari uji klinik tersebut, BPOM telah mengevaluasi dan menunjukkan hasil yang mendukung untuk dilakukan tahapan uji klinik berikutnya yaitu uji klinik fase III," kata dia.
"Selain Indonesia, uji klinik fase III ini juga akan dan sedang dilaksanakan di Brazil, Chili, Bangladesh dan Turki," katanya.
Baca juga: Presiden tinjau fasilitas pelaksanaan uji klinis vaksin COVID-19
Baca juga: Erick optimistis uji klinis vaksin Sinovac fase tiga berjalan baik
Penny mengatakan salah satu tugas dan fungsi BPOM sebagai otoritas obat adalah melakukan uji klinis pengawasan. Oleh karena itu, BPOM akan melakukan pengawalan terhadap pelaksanaan uji klinik.
Uji klinik, kata dia, dimulai dari pemberian Persetujuan Pelaksanaan Uji Klinik (PPUK) dan inspeksi Cara Uji Klinik yang Baik (CUKB). Inspeksi Cara Uji Klinik yang Baik untuk memastikan pelaksanaan uji klinik sesuai dengan protokol dan prinsip-prinsip CUKB, terutama bagi peneliti dan sponsor.
"Pelaksanaan uji klinik yang baik akan menghasilkan data yang valid dan dapat dipertanggungjawabkan secara etik dan ilmiah sebagai produk yang aman, bermutu dan memiliki khasiat. Hal tersebut menjadi tugas BPOM dalam mengawal khasiat dan keamanan obat sebelum dan sesudah beredar," kata dia.
Penny berharap masyarakat dapat berperan aktif dengan menjadi konsumen yang lebih bijak dalam menyikapi berbagai informasi terutama dari media sosial terkait COVID-19.
"Jangan mudah percaya dengan informasi yang berasal dari sumber yang tidak dapat dipertanggungjawabkan," katanya.
Baca juga: 19 relawan sudah disuntikkan vaksin COVID-19 di RSP Unpad Bandung
Baca juga: Ridwan Kamil resmi daftar jadi relawan uji klinis vaksin COVID-19
Pewarta: Anom Prihantoro
Editor: Budhi Santoso
Copyright © ANTARA 2020