Di Solidarity Trial ini kita tidak mengembangkan obat dari awal, karena kita tahu itu butuh waktu lama, tetapi kita sudah punya kandidat obat yang selama ini bermanfaat untuk penyakit sejenis, misalnya ebola, MERS, dan obat-obatan itu sudah diujicoba
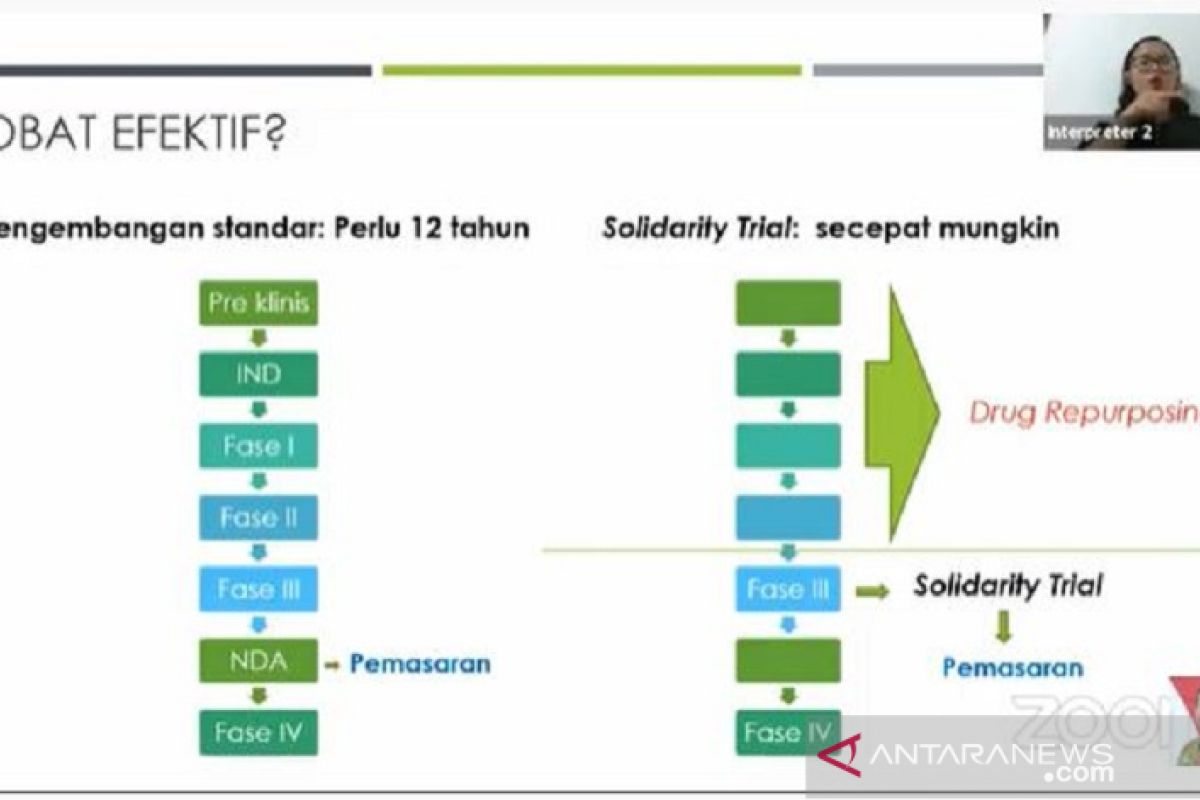
Jakarta (ANTARA) - Program "Solidarity Trial" atau uji obat COVID-19 yang dikoordinasi Organisasi Kesehatan Dunia (WHO) dan diikuti oleh ratusan negara, termasuk Indonesia, berupaya mempercepat proses pengujian dan penentuan obat dari waktu standar 12 tahun menjadi secepat mungkin.
Pernyataan itu disampaikan Kepala Pusat Penelitian dan Pengembangan Sumber Daya dan Pelayanan Kesehatan Kementerian Kesehatan Republik Indonesia, Irmansyah saat sesi seminar yang diselenggarakan Kementerian Luar Negeri via video konferensi di Jakarta, Jumat.
"Jika kita melakukan uji untuk menemukan obat baru sehingga dia dapat dipakai untuk misalnya kondisi pandemi ini, standarnya itu membutuhkan waktu rata-rata 12 tahun. [...] Di Solidarity Trial ini kita tidak mengembangkan obat dari awal, karena kita tahu itu butuh waktu lama, tetapi kita sudah punya kandidat obat yang selama ini bermanfaat untuk penyakit sejenis, misalnya ebola, MERS, dan obat-obatan itu sudah diujicobakan dan ada di pasaran," terang Irmansyah yang juga menjabat sebagai Koordinator Nasional untuk WHO.
Setidaknya, ada empat obat-obatan yang telah memasuki uji klinik atau uji coba fase 3 untuk pengobatan COVID-19. Uji klinik merupakan tahapan pengujian khasiat obat kepada manusia.
Empat obat yang diuji coba di antaranya, Remdesivir yang digunakan untuk mengobati pasien Ebola; Lopinavir/Ritonavir, obat HIV; Interferon beta-1a, obat sklerosis berlapis; terakhir Chloroquine dan hydroxychloroquine, obat Malaria.
Menurut Irmansyah, para pakar WHO berupaya menguji coba empat obat-obatan itu untuk COVID-19, kegiatan yang disebut drug repurposing. Oleh karena itu, tahapan pengembangan obat COVID-19 dalam solidarity trial tidak perlu melewati seluruh fase standar, seperti masa pre-klinis, pengenalan obat baru (initial new drug/IND), fase 1 (menguji keamanan obat), dan fase 2 (penentuan dosis obat).
Baca juga: Jerman perkirakan vaksin COVID-19 siap akhir tahun ini
Baca juga: AS tuding 'aktor siber' terkait China berupaya mencuri riset COVID-19
Empat obat-obatan itu langsung masuk tahap uji coba klinik atau fase 3 dan fase 4 atau tahapan terakhir dalam proses penentuan pengobatan. Dalam proses "solidarity trial", proses uji coba juga tidak melalui proses pemasaran (NDA).
Menurut Irmansyah, Indonesia termasuk salah satu negara yang aktif dan cepat dalam mengikuti program Solidarity Trial. "Kita salah satu negara pertama yang bergabung untuk wilayah WHO di Asia Tenggara dan secara internasional kita yang keenam atau ketujuh dari seluruh negara terlibat ," tambah dia.
Setidaknya saat ini ada 22 rumah sakit di Indonesia yang bergabung dalam tahapan uji klinik obat COVID-19 itu.
WHO pertama kali mengumumkan program Solidarity Trial ke publik pada 18 Maret 2020. Tujuan utama uji coba klinik obat-obatan itu untuk mengetahui keampuhan obat mencegah pasien COVID-19 meninggal dunia dan memeriksa efektivitas obat mengurangi gejala penyakit, serta pengaruhnya terhadap penggunaan ventilator (alat bantu pernapasan), dan waktu perawatan pasien.
Baca juga: Indonesia terima Rp1,2 T dari dunia internasional tanggulangi COVID-19
Baca juga: Organisasi internasional minta vaksin COVID-19 bebas paten dan murah
Pewarta: Genta Tenri Mawangi
Editor: Fardah Assegaf
Copyright © ANTARA 2020